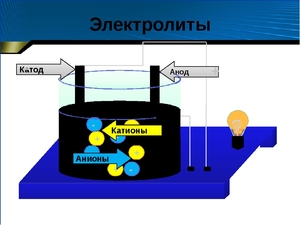
Хорошо известно, что одни вещества в растворенном или расплавленном состоянии проводят электрический ток, другие в тех же условиях ток не проводят. Это можно наблюдать с помощью простого прибора. Он состоит из угольных стержней (электродов), присоединенных проводами к электрической сети. В цепь включена электрическая лампочка, которая показывает присутствие или отсутствие тока в цепи. Если опустить электроды в раствор сахара, то лампочка не загорается. Но она ярко загорится, если их опустить в раствор хлорида натрия.
Вещества, распадающиеся на ионы в растворах или расплавах и потому проводящие электрический ток, называются электролитами.
Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
Содержание:
Неэлектролиты
Неэлектролиты находятся в растворе в виде неполярных или малополярных молекул.
К неэлектролитам относятся вещества с ковалентной неполярной (слабополярной) связью. В качестве примера веществ, не диссоциирующих в растворах и расплавах, можно привести простые вещества неметаллов (сера, фосфор, йод и др.), оксиды, органические кислоты (уксусная, молочная, муравьиная, лимонная и т. п.), органические спирты (этиловый спирт, глицерин и т. д.); также неэлектролитами являются такие вещества, как сахароза, ацетон, метан и другие.

Электролиты
Электролиты распадаются в растворе или расплаве на ионы, и именно наличие ионов способствует прохождению электрического тока. Процесс этот — распада на ионы — называют диссоциацией, а теория, описывающая данные процессы — теорией электролитической диссоциации. В растворе распад на ионы происходит по причине разрыва связей вещества, что является результатом взаимодействия с молекулами воды (то есть происходит гидратация электролита).
Ионы (атомы или их группы, обладающие отрицательным или положительным зарядом) под действием электрического тока начинают двигаться по направлению к одному из электродов, что и обуславливает электропроводимость.
Молекула электролита, способная диссоциировать на большее, чем два, количество ионов, будет диссоциировать постадийно. Примером может служить диссоциация многоосновной кислоты.
Подробнее познакомиться с теорией электролитической диссоциацией вы сможете, посмотрев это видео.
Степень диссоциации
Понятие, количественно характеризующее, насколько полно произошёл распад электролита на ионы, называют степенью диссоциации. Этот показатель рассчитывается как отношение количества продиссоциировавших молекул к общему числу молекул вещества в растворе и фактически показывает долю (процент) распавшихся на ионы молекул в общем количестве.

Следующие факторы могут влиять на степень электролитической диссоциации:
Температура
Зависимость от температуры достаточно сложна. Если распад на ионы экзотермический, то повышение температуры степень диссоциации будет уменьшать, а если эндотермический, повышение температуры приведёт к увеличению степени диссоциации. В целом же для каждого электролита есть определённые температурные условия, в которых он в максимальной степени будет распадаться на ионы.
Изменение показателя константы диссоциации (характеризует способность распадаться на ионы) для уксусной кислоты при изменении температуры можно привести в качестве примера:
| 0 °С | 25 °С | 50 °С |
| 1,65∙10-5 | 1,75∙10-5 | 1,62∙10-5 |
максимальная ионизация раствора, как видно, наступает при 25 °C, а при температурах выше и ниже этого значения диссоциация происходит в меньшей степени.
Что такое степень диссоциации? Подробный ответ вы найдете в этом видео.
Природа растворителя и электролита
Концентрация:
- Растворители с полярными молекулами, хорошей диэлектрической проницаемостью (этот показатель максимален у воды и равен 81, а, например, у этилового спирта — 25) обладают высокой ионизирующей способностью, то есть способны вызывать диссоциацию вещества.
- Вещества с сильно полярными ковалентными и ионными связями являются сильными электролитами.
- При увеличении концентрации степень диссоциации уменьшается и наоборот.
Стадия процесса диссоциации
Если молекула распадается на ионы постадийно, то каждая следующая стадия имеет примерно в 1000−10 000 раз меньший эффект, чем предыдущая.
Экспериментально определить степень диссоциации можно по электропроводности растворов, т. к. она прямо зависит от концентрации движущихся ионов. Истинное значение при этом получить нельзя, такое значение называют кажущимся. Оно меньше истинного, так как при движении к электродам ионы могут сталкиваться, что частично уменьшает их подвижность. При высокой концентрации может возникать притяжение между ионами, обусловленное электростатическими силами, они чаще сталкиваются, теряя свою подвижность, что влияет на показания электропроводности.
Например, в растворе соляной кислоты (1 моль/л) измерения покажут степень распада на ионы равной 0,78 (78%), но фактически раствор не будет содержать 22% недиссоциированных молекул, так как практически все молекулы диссоциированы.
Сильные и слабые проводники
По величине показателя степени диссоциации, выделяют электролиты сильные и слабые. К сильным условно относят вещества, значение степени диссоциации у которых больше 30%, если данный показатель ниже 5%, то к слабым, остальные считаются электролитами средней силы.
Сильные электролиты:
- соли;
- кислоты: хлорная, азотная, йодоводородная, хлорноватая, хлороводородная, серная, бромоводородная, марганцовая;
- основания: гидроксиды щелочных и щелочноземельных металлов.
Слабые электролиты:
- органические кислоты (все), как и кремниевая, сероводородная, угольная, синильная и некоторые другие.
- основания, например, гидроксид цинка II, гидроксид аммония, гидроксид меди II, гидроксид алюминия III, гидроксид магния II.
Видео
Из этого видео вы узнаете о свойствах электролитов.